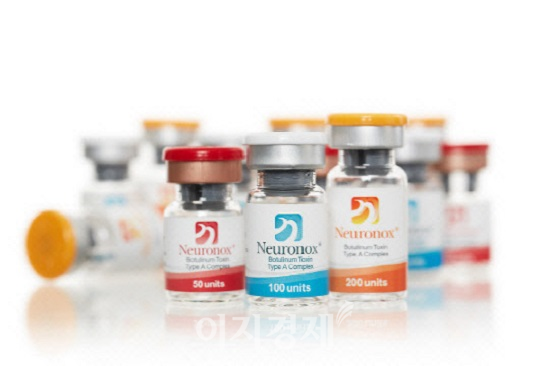
[이지경제] 김주경 기자 = 식품의약품안전처는 메디톡스 오송 3공장에서 수거한 수출용 보툴리눔 톡신 ‘메디톡신’(수출명 뉴로녹스) 보관검체(샘플)을 검사한 결과, 품질 부적합 판정을 내렸다고 17일 밝혔다.
식약처는 해당 제품에 대한 강제 회수·폐기 명령을 내리는 한편 유효기한이 다른 제품과 국내용 제품에 대해서도 추가 조사를 진행할 예정이다.
식약처에 따르면 유효기한이 이달 5일‧11일‧18일인 메디톡신 수출용 제품이 품질 부적합 판정을 받았다. 식약처의 이번 조치는 지난 8월 말경 메디톡스 오송 3공장을 방문해 메디톡신 검체를 수거해 검사하는 과정에서 밝혀졌다.
현재 식약처가 적발한 부적합 제품 갯수와 정확한 회수 물량은 파악되지 않았다.
업계에 따르면 수만 바이알(약병)에 달할 것으로 보인다. 보통 오송 3공장의 1개 배치에서는 메디톡신 2만5000바이알을 생산하고 있다.
해외 소비자들 중 문제 제품을 피부에 주입한 환자가 있는지도 확인되지 않았다.
이에 메디톡스는 식약처의 명령에 따라 해외에서 해당 제품이 얼마나 유통되는지와 피해현황을 파악해 수량을 명시한 회수계획서를 제출해야 한다.
앞서 메디톡스 전 직원 A씨는 메디톡스가 지난 2017년 오송 3공장을 신설하는 과정에서 메디톡신 품질검사 결과가 부적합으로 판정되자 자료를 조작했다는 내용을 국민권익위원회와 식약처에 신고한 바 있다.
이에 식약처는 올해 8월 오송 3공장에서 메디톡신 검체를 수거한 것.
수출용 3개 배치에서 생산된 보관검체를 검사해보니 의약품 용액의 작용세기인 '역가'와 제품 속 습기인 '함습도' 품질이 부적합했다. 배치는 생물학적 제제가 생산시설에서 한 번에 생산된 단위를 의미한다.
식약처 관계자는 “문제 제품은 즉시 회수·폐기하고 추가 조사를 진행해 메디톡스의 행정처분 수위를 정해 적극적으로 조치하겠다”며 “유효기간이 다른 제품들도 추가로 검사할 예정”이라고 말했다.
한편 이날 메디톡스는 홈페이지를 통해 “이번 회수조치와 관련해 자체적으로 의약품의 하자 유무 등 사실관계를 조사하는 한편 관련 업체와 협의해 회수 절차를 진행하겠다”며 “지속적인 모니터링을 통해 재발 방지에도 최선을 다하겠다”고 밝혔다.
메디톡신은 메디톡스가 2006년 3월 국산 첫 보툴리눔 톡신 제제로 식약처로부터 허가를 받은 제품이다.
김주경 기자 ksy055@ezyeconomy.com