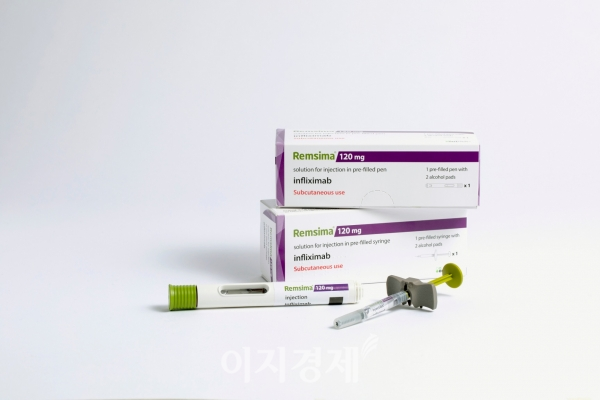
[이지경제] 이민섭 기자 = 셀트리온은 세계 최초 인플릭시맙 피하주사 제제 ‘램시마SC’가 현지시간 25일 유럽의약품청(EMA)으로부터 판매 승인을 획득했다고 26일 밝혔다.
램시마SC는 렘시마를 기존 정맥주사에서 피하주사로 제형을 변경해 자체 개발한 바이오의약품이라는 설명이다. EMA는 심사 과정부터 ‘바이오베터’ 형식인 확장 신청이라는 기존 바이오시밀러와 차별화된 승인 절차를 밟았다.
앞서 셀트리온은 지난해 11월 EMA에 렘시마SC 시판 허가를 신청한 지 12개월 만에 판매 승인을 획득해 제형 몇경 및 성능 개선을 통한 바이오베터로서의 상품성을 입증하고 기술력을 인정받았다. 특히 약 130개국에 특허출원을 완료할 예정이기 때문에 향후 20년 동안 인플릭시맙 피하주사시장을 독점할 것으로 보인다.
셀트리온은 이번 승인을 통해 바이오시밀러 선도기업에서 한 단계 진화한 글로벌 신약개발회사로 도약할 수 있는 발판을 마련한 것으로 기대하고 있다. 특히 램시마SC는 바이오베터라는 독점적 지위를 이용, 가격 측면에서 1차 치료제(휴미라, 엔브렐, 레미케이드 등) 보다 더 높은 가격에 판매할 수 있는 ‘프라임 시밀러’ 전략 구사가 가능해져 수익성 향상에 큰 기여를 할 것이라는 평가다.
셀트리온은 이번에 램시마SC가 승인 받은 RA적응증에 추가해 내년 중반까지 IBD를 포함한 자가면역질환 적응증 전체에 대해 승인을 획득한다는 계획이기에 내년 하반기부터 램시마SC의 시장 침투는 더욱 가속화 될 전망이다.
셀트리온헬스케어는 주요 유럽 시장에 이미 설립한 14개 법인 및 지점을 잇는 자체 직판망을 활용해 램시마SC를 판매할 예정이다. 2020년 2월 독일을 시작으로 3월부터는 영국, 네덜란드 등 주요 시장에서 램시마SC를 순차 출시해 2020년 연말까지 유럽 전역으로 제품 판매를 확대한다는 계획이다.
이밖에 내년 상반기까지 총 6조4000억원 규모의 유럽 TNF-α 억제제 시장에 진출하고, 2020년말까지 유럽 전체 TNF-α 억제제 시장의 90%에 해당하는 9조 2천억원 규모의 시장에 램시마SC를 선보인다.
셀트리온 관계자는 “셀트리온은 세계 유수의 학회를 통해 램시마SC 임상 결과를 발표하고 안전성과 효능을 입증했으며, 이를 바탕으로 램시마SC의 시장 진입에 대해 유럽 의료진들의 큰 기대를 확인할 수 있었다”면서 “셀트리온헬스케어는 램시마SC의 시판을 계기로 유럽 시장에서 다른 바이오시밀러와 차별화된 프라임급 위치에서 시장점유율을 확대하고, 바탕으로 램시마SC가 매출 증대와 수익성 개선에도 큰 몫을 할 것”이라고 말했다.
이민섭 기자 minseob0402@ezyeconomy.com