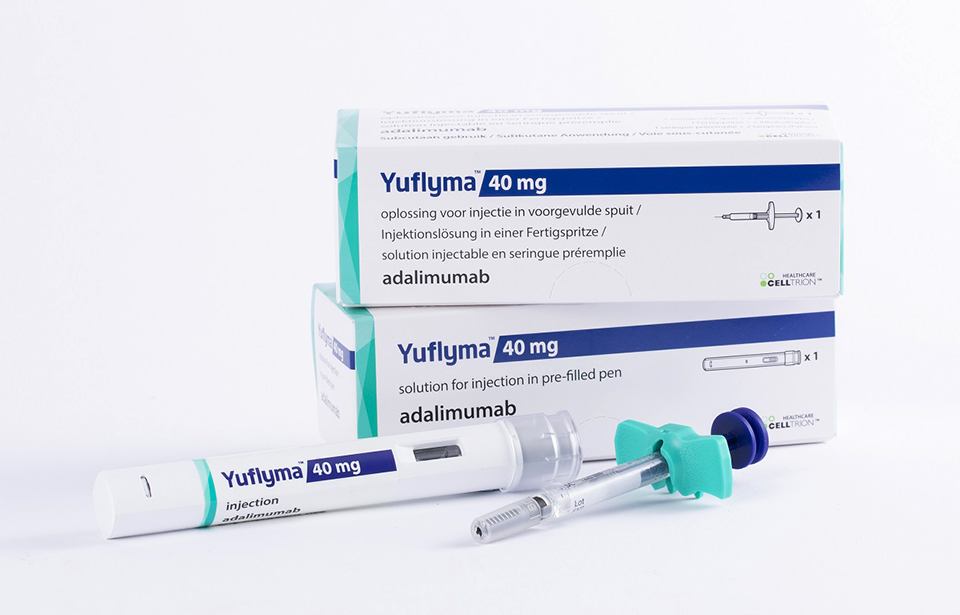
[이지경제=윤현옥 기자] 셀트리온이 자가면역질환 치료제 ‘유플라이마’ 의 유럽 판매허가를 받았다.
셀트리온은 유럽의약품청(EMA) 산하 약물사용자문위원회(CHMP)로부터 자가면역질환 치료제 ‘휴미라’(성분명 아달리무맙)의 바이오시밀러(복제약) ‘유플라이마’ 80㎎/0.8㎖ 용량 제형에 대해 판매허가를 받았다고 22일 밝혔다.
이번 허가는 작년 12월 추가 판매승인 권고의견을 받은 지 약 2개월 만이다. 이에 따라 셀트리온은 40㎎/0.4㎖과 80㎎/0.8㎖ 두 종류의 제품을 유럽에 공급할 수 있게 됐다.
유플라이마는 작년 2월 EMA로부터 허가를 획득해 출시한 세계 최초의 고농도 제형 휴미라 바이오시밀러로, 류마티스 관절염(RA)과 염증성 장질환(IBD), 건선(PS) 등 휴미라가 보유한 모든 적응증에 대해 유럽시장 내 판매를 개시했다. 작년 10월에는 한국 식품의약품안전처로부터 허가를 획득하고 국내 시장 출시도 준비하고 있다. 셀트리온은 이번 유럽에서의 유플라이마 용량제형 추가 승인으로 폭넓은 처방이 가능해짐에 따라 시장도 더 확대될 것으로 기대하고 있다.
유플라이마의 오리지널의약품인 휴미라는 미국 제약사 애브비(Abbvie)가 개발한 블록버스터 바이오의약품으로, 세계 시장에서 단일 품목 매출 1위를 기록하고 있다.
대웅제약, 당뇨 신약 ‘이나보글리플로진’ 中 임상 3상 승인
대웅제약이 중국 국가의약품감독관리국으로부터 SGLT-2 억제 기전의 당뇨병 신약 ‘이나보글리플로진’의 메트포르민 병용요법에 대한 임상 3상을 허가받았다.
지난해 11월 임상시험신청서(Clinical Trial Application, CTA)를 제출한지 3개월 만이다.
대웅제약은 중국에서 2형 당뇨병 환자들을 대상으로 이나보글리플로진과 기존 당뇨병 치료제 메트포르민 병용요법의 임상 3상을 진행할 계획이다.
올 1월 국내에서 유사하게 실시한 임상 3상 톱라인(주요) 결과에 따르면, 이나보글리플로진과 메트포르민 병용요법은 다파글리플로진과 메트포르민 병용요법과 비교해 비열등성을 입증했다. 대웅제약은 중국에서도 이나보글리플로진의 임상적 가치를 인정받아 2025년까지 허가를 취득한다는 계획이다.
이나보글리플로진은 대웅제약이 국내 제약사 중 최초로 개발 중인 SGLT-2 억제 당뇨병 치료 신약이다. 국내에서 실시된 단독, 메트포르민 2제 병용, 메트포르민과 DPP4 억제제 3제 병용 3상 시험에서 혈당이 적절히 조절되지 않는 제2형 당뇨병 환자 총 630명 대상으로 이나보글리플로진의 유효성과 안전성을 확인한 바 있다. 대웅제약은 오는 2023년 국내 발매를 목표로 하고 있다.
휴젤, 보툴리눔 톡신 ‘레티보’ 오스트리아 허가 획득
휴젤은 이달 18일(현지시간) 오스트리아 연방보건안전청(BASG)에서 미간주름 개선 보툴리눔 톡신 ‘레티보’의 품목허가를 획득했다.
앞서 휴젤은 지난달 25일 유럽의약품안전관리기구연합체(HMA)로부터 레티보에 대한 품목허가 승인 권고 의견을 받았다. 이를 기반으로 즉시 유럽 11개국 국가별 승인 절차에 돌입했다.
이후 지난 달 27일 프랑스에서 가장 먼저 품목허가 절차를 완료하고 국내 톡신 기업 최초의 유럽 론칭을 앞두고 있다.
휴젤은 1분기 내 레티보의 선적 및 현지 주요 시장에서의 론칭을 목표로 하고 있다. 내년까지 유럽 36개국 진출을 완료할 계획이다. 유럽은 중국, 미국과 함께 전 세계 80%를 차지하고 있는 5000억원 규모의 보툴리눔 톡신 시장으로, 2025년까지 연평균 10%의 성장이 전망되고 있다.
휴젤 관계자는 “레티보의 검증된 품질과 안전성을 바탕으로 유럽 시장에서의 입지 확대에 주력할 예정”이라고 말했다.
- ‘헬시플레저’ 열풍에 건강한 다이어트 제품 인기
- 동아제약, 동아쏘시오홀딩스 올해 사상 최고 실적 이끈다
- 동국제약, 반려견 영양간식 ‘캐니비타 올인원 덴탈츄’ 출시 外
- 한올바이오파마, 신약개발 전문가 차비 박사 영입
- GC녹십자, 작년 영업익 전년比 47%↑…해외시장서 상승세 이어간다
- 한미 희귀질환 신약, SCI 국제학술지 표지 논문 등재 外
- 한미약품, 작년 코로나19 ‘완벽’ 극복…호실적 달성
- 삼성바이오로직스, ‘탄소경영 아너스’ 획득 外
- 닥스키즈·블루독, 아동복시장 두고 새학기 대전
- JW중외제약, 휴젤, 한영세미나…도약 준비하는 바이오업계
- [이지경제 뉴스데스크] SK, 코로나19서 ‘선방’