전년 대비 월평균 91.1% 수준…허가 심사 투명성 강화 기조 지속
희귀의약품·신개발 의료기기 포함…신속 허가로 환자 치료기회 확대
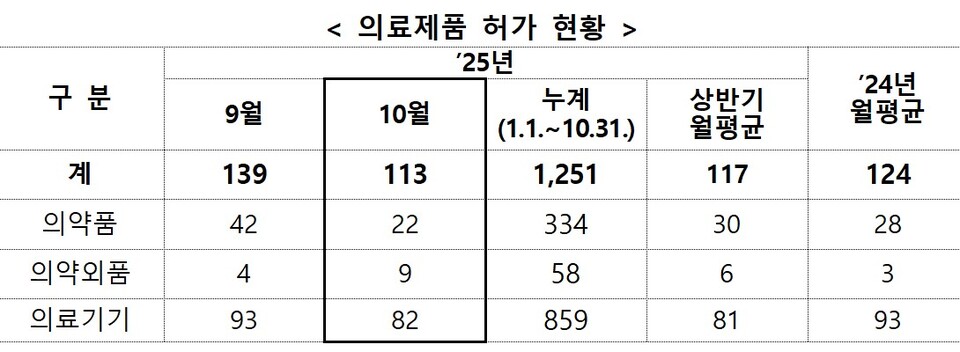
식품의약품안전처는 지난 10월 한 달간 총 113개 의료제품을 허가했다고 21일 밝혔다. 허가 품목은 의약품 22개, 의약외품 9개, 의료기기 82개로 구성됐다.
이는 지난해 월평균 허가 건수(124개) 대비 91.1% 수준, 올해 상반기 월평균(117개) 대비 96.6% 수준이다. 특히 신약과 자료제출의약품, 생물학적제제 등 주요 의약품과 더불어, 신개발·희소의료기기 등 다양한 분야의 제품이 신규 허가를 받았다.
의약품 부문에서는 희귀의약품 ‘닌테브연질캡슐150mg(닌테다닙에실산염)’이 만성 섬유성 간질성 폐질환 치료제로 승인됐다. 의료기기 부문에서는 손목터널증후군 수술 시 피부 절개 없이 경피적 방식으로 횡수근관인대를 절제하는 ‘의료용 박리자(Smartwire CTR)’가 허가되면서 치료 접근성 확대가 기대된다.
식약처는 “안전하고 유효한 제품을 신속하게 허가해 환자의 치료 기회를 넓히는 한편, 의료제품 허가 현황을 정기적으로 제공해 허가심사의 투명성과 신뢰성을 강화해 나갈 것”이라고 밝혔다.